Термодинамика

Два баллона, объёмами 60 л и 40 л, наполнены Неоном 80 г и Гелием 32 г соответственно. После соединения баллонов давление внутри 300 кПа. Определите температуру газов в конце процесса.
“Досрочная волна 2019 вариант 1”
301
Найдем количество газов. Количество неона: \[\nu_{N}=\dfrac{80\text{ г}}{20\text{ г/моль}}=4\text{ моль}\] Количество гелия: \[\nu_H=\dfrac{32\text{ г}}{4\text{ г/моль}}=8\text{ моль}\] Конечную температуру можно найти из уравнения Клапейрона–Менделеева: \[p(V_N+V_N)=(\nu_N+\nu_H)RT' \Rightarrow T'=\dfrac{p(V_N+V_H)}{(\nu_N+\nu_H)R}=\dfrac{300\text{ кПа}100\text{ л}}{12\text{ моль}\cdot 8,32\text{ дж/(К$\cdot$ моль)}}\approx 301\text{ К}\]
Постоянную массу идеального одноатомного газа изобарно сжали так, что \(T_2=\dfrac{T_1}{k}\) Затем этот же газ адиабатически расширяется так, что \(T_3=\dfrac{T_2}{2}\) Отношение модулей работ в изобарном и адиабатическом процессах \(n=4\) Найдите \(k\).
“Основная волна 2019”
При изобарном сжатии над гахов совершается работа, модуль которой \(A_1=|p\Delta V|\) где \(p\) – давление гелия в этом процессе, \(\Delta V\) – изменение его объёма.
В соответствии с уравнением Менделеева–Клапейрона для этого процесса можно записать: \[p\Delta V =\nu R (T_1-T_2)=A_1\] В адиабатном процессе (процессе без теплообмена) в соответствии с первым законом термодинамики сумма изменения внутренней энергии газа и его работы равна нулю: \[\dfrac{3}{2}\nu R (T_3-T_2)+A_2=0\] При записи последнего соотношения учтено выражение для изменения внутренней энергии идеального одноатомного газа: \[\Delta U =\dfrac{3}{2}\nu R (T_3-T_2)\] Преобразуя записанные уравнения с учётом соотношений температур, заданных в условии задачи, получаем: \[A_1=\nu RT_2(k-1)\hspace{5 mm}A_2=\dfrac{3}{4}\nu RT_2\] По условию \(\dfrac{A_1}{A_2}=n=4\) Следовательно \[\dfrac{4\nu RT_2(k-1)}{3\nu R T_2}=4 \Rightarrow 4k-4=12 \Rightarrow 4k=16 \Rightarrow k=4\]
В вертикальном цилиндре, закрытом лёгким поршнем, находится этиловый спирт (\(C_2H_6O\)) при температуре кипения \(t = 78^\circ C\). При сообщении спирту количества теплоты \(Q\) часть его превращается в пар, который при изобарном расширении совершает работу A. Удельная теплота парообразования спирта \(L = 846 \cdot 10^3\) Дж/кг, а его молярная масса – 46\(\cdot 10^{-3}\) кг/моль. Какая часть подведённого к этиловому спирту количества теплоты переходит в работу? Объёмом жидкого этилового спирта пренебречь.
“Основная волна 2020 Вариант 2”
Количество теплоты, полученное системой равно \[Q=L\Delta m,\quad (1)\] где \(\Delta m\) – масса образовавшегося пара.
Так как процесс испарения прошел не до конца, то данный процесс изотермический, а значит изменение внутренней энергии будет за счет изменения массы пара \[A=\dfrac{\Delta m}{M}RT,\quad (2)\] где \(T\) – температура газа в Кельвинах.
Объединим (1), (2) и (3) и найдем отношение \(\dfrac{A}{Q}\) \[\dfrac{A}{Q}=\dfrac{\dfrac{\Delta m}{M}RT}{L\Delta m}=\dfrac{RT}{LM}=\dfrac{ \cdot 8,31 \text{ Дж/(К$\cdot$моль)}\cdot 351\text{ К}}{846\cdot 10^3\text{ Дж/кг}\cdot 46\cdot 10^{-3}\text{ кг/моль}} \approx 0,075\]
Сосуд объемом \(V=10\) л содержит \(\nu=5\) моль гелий при температуре \(t=17^\circ C\). Если сообщить гелию количество теплоты \(Q=3\) кДж, то сосуд лопнет. Какую максимальную разность давлений внутри сосуда и снаружи него он выдерживает? Атмосферное давление \(p_0=10^5\) Па.
“Основная волна 2020 Вариант 3”
Запишем уравнение Клапейрона – Менделеева \[p_{max}V=\nu R T_{max} \quad (1)\] где \(p_{max}\) и \(T_{max}\) – максимальные давление и температура газа соответственно.
Газ в процессе подвода тепла не увеличивает объем, поэтому работа газа в данном процессе равна 0, следовательно, первый закон термодинамики запишется в виде: \[Q=\Delta U=\dfrac{3}{2}\nu r (T_{max}-T_{0})\] Выразим отсюда конечную температуру: \[T_{max}=\dfrac{2Q}{3\nu R}+T_0\] Подставим конечную температуру в (1) и выразим давление \[p_{max}=\dfrac{2Q}{3V}+\dfrac{\nu R T_0}{V}=\] Откуда разность давлений \[\Delta p=p_{max}-p_0=\dfrac{2\cdot 30000\text{ Дж}}{3\cdot 10^{-2}\text{ м$^3$}}+\dfrac{5\text{ моль}\cdot 8,31\text{ Дж/(моль$\cdot$ К)}\cdot 290\text{ К}}{10^{-2}\text{ м$^3$}}-10^5\text{ Па}=1'304'950\text{ Па}\]
Гелий в количестве \(\nu\) = 3 моль изобарно сжимают, совершая работу \(A_1\) = 2,4 кДж. При этом температура гелия уменьшается в 4 раза: \(T_2=\dfrac{T_1}{4}\) . Затем газ адиабатически расширяется, при этом его температура изменяется до значения \(T_3=\dfrac{T_1}{8}\). Найдите работу газа \(A_2\) при адиабатном расширении. Количество вещества в процессах остаётся неизменным.
“Демоверсия 2020”
При изобарном сжатии над гелием совершается работа, модуль которой \(A_1=|p\Delta V|\) где \(p\) – давление гелия в этом процессе, \(\Delta V\) – изменение его объёма.
В соответствии с уравнением Менделеева–Клапейрона для этого процесса можно записать: \[p\Delta V =\nu R (T_1-T_2)\] В адиабатном процессе (процессе без теплообмена) в соответствии с первым законом термодинамики сумма изменения внутренней энергии газа и его работы равна нулю: \[\dfrac{3}{2}\nu R (T_3-T_2)+A_2=0\] При записи последнего соотношения учтено выражение для изменения внутренней энергии идеального одноатомного газа: \[\Delta U =\dfrac{3}{2}\nu R (T_3-T_2)\] Преобразуя записанные уравнения с учётом соотношений температур, заданных в условии задачи, получаем: \[A_1=3\nu RT_2\hspace{5 mm}A_2=\dfrac{3}{4}\nu RT_2\] Получаем: \[A_2=\dfrac{A_1}{4}=600\text{ Дж}\]
В вертикальном цилиндре, закрытом лёгким поршнем, находится бензол (\(C_6H_6\)) при температуре кипения \(t=80^\circ C\) . При сообщении бензолу количества теплоты \(Q\) часть его превращается в пар, который, при изобарном расширении, совершает работу \(A\). Удельная теплота парообразования бензола \(396\cdot 10^3\text{ Дж/кг}\), его молярная масса \(78\cdot 10^{-3}\text{ кг/моль}\) кг/моль. Какая часть подведённого к бензолу количества теплоты переходит в работу? Объёмом жидкого бензола пренебречь.
“Демоверсия 2021”
Количество теплоты, полученное системой равно \[Q=L\Delta m,\quad (1)\] где \(\Delta m\) – масса образовавшегося пара.
Так как процесс испарения прошел не до конца, то данный процесс изотермический, а значит изменение внутренней энергии будет за счет изменения массы пара \[A=\dfrac{\Delta m}{M}RT,\quad (2)\] где \(T\) – температура газа в Кельвинах.
Объединим (1), (2) и (3) и найдем отношение \(\dfrac{A}{Q}\) \[\dfrac{A}{Q}=\dfrac{\dfrac{\Delta m}{M}RT}{L\Delta m}=\dfrac{RT}{LM}=\dfrac{ 8,31 \text{ Дж/(К$\cdot$моль)}\cdot 353\text{ К}}{ 396\cdot 10^3\text{ Дж/кг}\cdot 78\cdot 10^{-3}\text{ кг/моль}} = 9,5\%\]
С одним молем идеального одноатомного газа проводят циклический процесс 1-2-3-1, где 1-2 – адиабата, 2-3 – изобара, 3-1 – изохора. Температуры в точках 1, 2, 3 равны 600 К, 455 К и 300 К соответственно. Найдите КПД цикла.
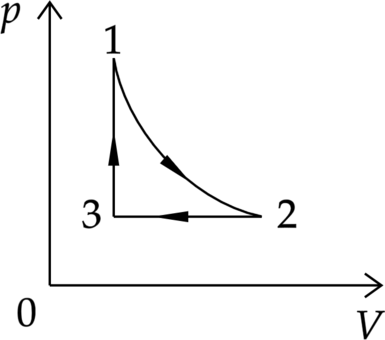
“Досрочная волна 2019 вариант 2”
Цикл не является циклом идеальной тепловой машины. Поэтому воспользуемся общей формулой через теплоту нагревателя и теплоту холодильника. \[\eta = \dfrac{Q_\text{н}-_\text{х}}{_\text{н}}=1-\dfrac{Q_\text{х}}{Q_\text{н}}\] Необходимо выяснить, на каком из участков цикла газ получает тепло от нагревателя, а на каком – отдаёт холодильнику. Для этого проведём подсчёт теплоты каждого участка по 1-му началу термодинамики \[Q=A+\Delta U\] 1. На участке 1–2 представлена адиабата — по определению количество теплоты на этом участке равно нулю: \(Q_{12}=0\) 2. На участке 2–3 представлен изобарный процесс. Тут нужно подсчитать и работу газа и внутреннюю энергию
\[Q_{23}=A_{23}+\Delta U_{23}=p_{2}\left(V_{3}-V_{2}\right)+\frac{3}{2} v R\left(T_{3}-T_{2}\right)=\] \[=\left(p_{2} V_{3}-p_{2} V_{2}\right)+\frac{3}{2} v R\left(T_{3}-T_{2}\right)=\left(v R T_{3}-v R T_{2}\right)+\frac{3}{2} v R\left(T_{3}-T_{2}\right)=\] \[=\frac{5}{2} v R\left(T_{3}-T_{2}\right)<0\] \[Q_\text{х}=\left|Q_{23}\right|=\frac{5}{2} v R\left(T_{2}-T_{3}\right)\] 3.На участке 3–1 объём газ постоянен, работа равна нулю: \[Q_{31}=A_{31}+\Delta U_{31}=\Delta U_{31}=\frac{3}{2} v R\left(T_{1}-T_{3}\right)>0\] Теплота получилась на этом участке положительной, а значит, газ получает теплоту от нагревателя \[Q_\text{н}=Q_{31}=\frac{3}{2} v R\left(T_{1}-T_{3}\right)\] 4. Найдём значение КПД: \[\eta=1-\frac{Q_\text{х}}{Q_\text{н}}=1-\frac{\sum_{2} v R\left(T_{2}-T_{3}\right)}{3 v R\left(T_{1}-T_{3}\right)}=1-\frac{5}{3} \cdot \frac{T_{2}-T_{3}}{T_{1}-T_{3}}\] \[\eta=1-\frac{5}{3} \cdot \frac{455-300}{600-300}=1-\frac{31}{36}=\frac{5}{36} \approx 0,139=13,9 \%\]



